Uji Iodium: Prinsip, Prosedur, Hasil, Kegunaan
Uji iodium adalah uji kimia yang digunakan untuk membedakan monosakarida atau disakarida dari polisakarida tertentu seperti amilase, dekstrin, dan glikogen. Ada variasi dari uji ini yang disebut uji pati-iodium, yang menunjukkan bahwa glukosa yang dibuat oleh tanaman ditemukan di daun tanaman.
Tujuan Uji Iodium
Uji iodium, atau sering disebut uji pati, adalah metode kimia yang digunakan untuk mendeteksi keberadaan polisakarida, khususnya pati, dalam suatu sampel. Tujuan utama dari uji ini adalah untuk mengidentifikasi keberadaan dan konsentrasi pati dalam berbagai bahan, seperti makanan, tumbuhan, atau bahan biologis lainnya.
Prinsip Uji Iodium
- Uji iodium didasarkan pada fakta bahwa ion poliiodida membentuk kompleks adsorpsi berwarna dengan rantai heliks residu glukosa: glikogen (coklat kemerahan), amilase (biru-hitam), atau dekstrin (hitam).
- Polisakarida, monosakarida, dan disakarida yang bercabang seperti selulosa tidak memiliki warna. Warna jingga-kuning dihasilkan oleh amilopektin.
- Uji iodium menggunakan iodium Lugol, larutan berair dari unsur iodium dan kalium iodida.
- Iodium sendiri tidak larut dalam air, namun, jika kalium ditambahkan, ion iodin bereaksi dengan iodin untuk membentuk ion triiodida, yang kemudian bereaksi dengan molekul iodin untuk membentuk ion pentaiodida.
- Larutan iodium berwarna coklat, tetapi ion iodin, triiodida, dan pentaiodida tidak berwarna.
- Rantai glukosa memiliki struktur heliks, yang dapat berupa kumparan atau pegas, yang sangat penting untuk pengujian ini.
- Selanjutnya, warna yang dihasilkan tergantung pada panjang rantai glukosa.
- Ion triiodida dan pentaiodida yang terbentuk bersifat linier dan berada didalam struktur heliks.
- perpindahan muatan antara heliks dan ion poliiodida mengubah jarak tingkat energi, yang dapat menyerap cahaya tampak, memberikan warna pada kompleks.
- Dengan peningkatan suhu, intensitas warna menurun, dan ada senyawa organik seperti etanol yang dapat bercampur dengan air.
- Kompleks amilase-yodium berwarna biru terdisosiasi saat dipanaskan, tetapi terbentuk lagi saat didinginkan karena struktur heliks terganggu. Akibatnya, amilosa kehilangan kapasitas untuk mengikat yodium, dan warna birunya hilang. Setelah dingin, kapasitas pengikatan yodium pulih, dan warna biru muncul kembali setelah struktur heliks terbentuk kembali.
Persyaratan Uji Iodium
1. Reagen
- Iodium Lugol: 5% iodium unsur dicampur dengan 10% kalium iodida untuk membentuk iodium Lugol.
- Sampel uji
2. Alat
- Tabung reaksi
- Rak tabung reaksi
3. Bahan
- Air
Prosedur Uji Iodium
- Ambil 1 ml sampel yang diberikan dalam tabung reaksi yang bersih dan kering.
- Ambil 1 ml air sulingan dalam tabung lainnya.
- Tambahkan sekitar 2-3 tetes larutan Lugol ke kedua tabung kemudian diaduk.
- Amati munculnya warna dalam tabung reaksi.
- Panaskan tabung reaksi dalam penangas air sampai warnanya hilang.
- Keluarkan tabung reaksi untuk didinginkan
- Catatlah penampakan warna yang terlihat dalam tabung reaksi.
Hasil dan Interpretasi Uji Iodium
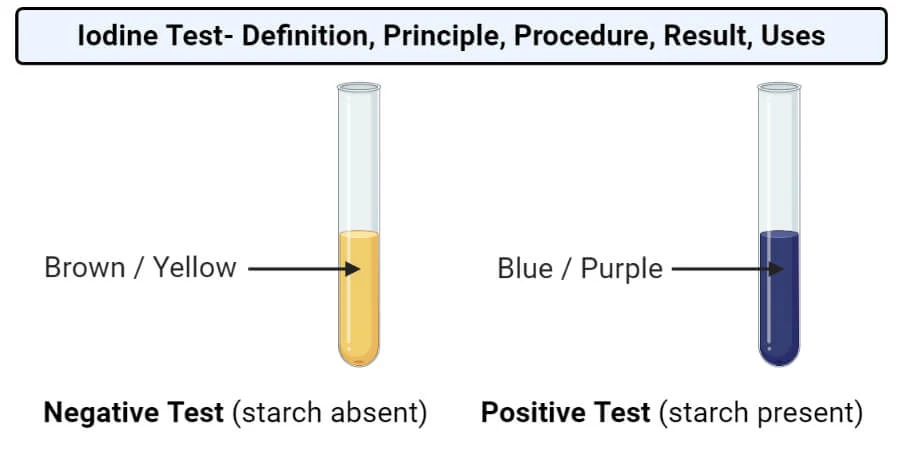
- Munculnya warna biru kehitaman atau ungu menunjukkan hasil positif, yang menandakan adanya pati.
- Jika tidak terjadi perubahan warna maka hasilnya negatif dan menandakan tidak adanya pati.
Penggunaan Uji Iodium
Uji iodium digunakan dalam berbagai bidang, antara lain:
- Industri Pangan: Untuk menguji kandungan pati dalam produk makanan seperti tepung, beras, dan kentang.
- Botani dan Pertanian: Untuk mengidentifikasi keberadaan pati dalam tanaman, yang dapat memberikan informasi mengenai aktivitas fotosintesis dan penyimpanan energi.
- Pendidikan: Sebagai alat pembelajaran untuk menunjukkan reaksi kimia dan identifikasi karbohidrat dalam laboratorium sekolah dan universitas.
- Penelitian Biokimia: Untuk mempelajari sifat-sifat pati dan interaksinya dengan zat lain.
- Demikian pula, pengujian ini dilakukan untuk menguji proses fotosintesis pada tumbuhan.
Keterbatasan Uji Iodium
Uji ini tidak dapat dilakukan dalam kondisi asam karena pati akan terhidrolisis dalam keadaan demikian. Dan Uji ini merupakan uji kualitatif dan tidak menandakan konsentrasi pati secara akurat.