Dehidrasi
Molekul air yang digunakan pada tahapan fiksasi dapat mengganggu tahapan selanjutnya dari proses pembuatan preparat (kecuali metode beku). Tahapan pembuangan air tersebut, disebut dengan tahapan dehidrasi. Untuk kebanyakan jaringan, tahapan dehidrasi diikuti dengan tahapan penjernihan (Clearing) sehingga jaringan menjadi jernih (transparan) sebelum diinfiltrasi. Melewatkan jaringan melalui satu seri larutan yang dapat menarik air dengan konsentrasi larutan semakin naik dan konsentrasi air semakin menurun. Larutan akan menarik air dan kemudian menempati ruangan yang ditinggalkan oleh air tersebut.
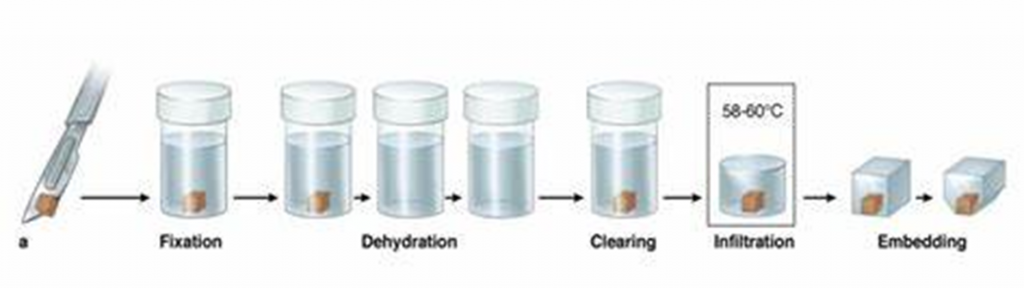
Tujuan Dehidrasi
- Menarik air dari dalam jaringan setelah difiksasi
- Mencuci dan memperkokoh jaringan yang keras dan rapuh
- Mencegah air menyebabkan pembusukan pada sampel jaringan
- Agar tahapan infiltrasi berhasil, air harus dihilangkan karena air tidak dapat bercampur dengan paraffin
- Mencegah air merusak tahapan pewarnaan
- Agar sampel yang disimpan dapat bertahan lama.
Bagaimana Specimen Didehidrasi?
- Dehidrasi tidak bisa dilakukan dengan cepat, harus dilakukan secara perlahan, bertahap, selangkah demi selangkah;
- Dehidrasi dilakukan dengan memperlakukan spesimen dengan konsentrasi meningkat larutan dehidran (misalnya etanol) secara berurutan;
- Spesimen ditempatkan (direndam) dalam larutan dehidran untuk jangka waktu tertentu;
- Interval waktu dehidrasi ditentukan oleh ukuran dan sifat spesimen;
- Perendaman spesimen dalam dehidran konsentrasi rendah terlalu lama membuat spesimen jaringan lunak;
- Perendaman spesimen dalam dehidran konsentrasi tinggi terlalu lama akan membuat jaringan lunak menjadi rapuh;
- Larutan dehidran digantik dengan menuangkannya dari botol spesimen;
- Setelah penuangan, botol spesimen segera diisi dengan konsentrasi larutan yang lebih tinggi;
- Spesimen tidak boleh mengering pada tahap apa pun.
Mekanisme Dehidrasi
- Air secara bertahap diekstraksi dari jaringan dengan melewatkannya ke alkohol bertingkat: 50% 70% 80% 95% 100%;
- Kondisi ini mencegah kerusakan mekanis pada struktur halus intrasel;
- Jika air diekstraksi dari jaringan terlalu cepatakan dapat memicu kerusakan jaringan;
Syarat Larutan Pendehidrasi
- Dapat menarik air dari dalam jaringan;
- Dapat bercampur dengan clearing agent (larutan penjernih);
- Tidak membatalkan fungsi fiksasi;
- Dapat mempertahankan bentuk jaringan seperti setelah difiksasi;
- Mampu mengisi ruangan pada jaringan yang ditinggalkan oleh air;
- Sebaiknya digunakan dalam keadaan segar.
Larutan Pendehidrasi
- Alkohol
- Merupakan larutan pendehidrasi yang umum digunakan.
- Dapat bercampur dengan xylol (clearing agent).
- Dimulai dari konsentrasi terendah hingga konsentrasi tertinggi (absolut).
- Pada konsentrasi dibawah 70% atau 80%, tidak boleh ditahan lebih dari 30-45 menit (kontiniu) pada masing-masing konsentrasi.
- Pada jaringan yang difiksasi dengan larutan Zenker dan Helly, pada konsentrasi alcohol 70%, tambahkan iodium tincture yang berfungsi untuk melarutkan merkuri klorida dari dalam jaringan.
- Pelepasan merkuri klorida ditandai dengan warna pada larutan pendehidrasi.
- Jika masih berwarna, ulangi penambahan iodium tincture hingga warna menjadi bening.
- Penggunaan alcohol absolut memiliki biaya produksi yang sangat tinggi. Maka dianjurkan untuk memproduksi alcohol 95%.
- Untuk membuat larutan alcohol 80% dari alcohol 95%, cukup campurkan 80% bagian alcohol 95% dengan 15 bagian aquades.
- Dioksan (kombinasi dehidrasi dan infiltrasi)
- Keuntungan
- Lebih praktis dan lebih cepat dibandingkan dengan alcohol
- Kualitas sayatan sebanding dengan dehidrasi alcohol
- Dapat bercampur dengan baik menggunakan air, alcohol, dan xylol
- Menghemat alcohol dan xylol
- Dapat bercampur dengan Canada balsam
- Harga lebih murah dibanding dengan xilol
- Pengerutan jaringan tidak terlalu signifikan dan dapat melarutkan merkuri
- Kerugian
- Bersifat toksik (beracun)
- Sangat mudah menguap, sehingga harus disimpan dalam botol tertutup rapat
- Sering mengandung air dan bahan lain sehingga kemurniannya berkurang
- Adanya air dan bahan lain menyebabkan pengerutan jaringan hingga 50%
- Berwarna keruh jika sudah mengandung air.
- Keuntungan
- Gliserin/Gliserol
- Gliserin adalah bahan yang sangat baik untuk dehidrasi bahan halus (misalnya: alga dan jamur)
- Titik didih = 290 derajat Celcius, sehingga air dapat dihilangkan dengan penguapan
- Kerugian: gliserin menyebabkan plasmolisis sel (untuk menghindari plasmolisis, lakukan dehidrasi dengan sangat perlahan dan bertahap)
- Prosedur:
- Hilangkan fiksatif dari jaringan (cuci dengan air)
- Rendam dalam gliserin 5% dalam stoples bermulut lebar
- Biarkan toples terbuka (untuk memudahkan penguapan air), untuk mempercepat penguapan: letakkan toples dalam suhu 35 oC
- Dehidrasi harus dilakukan di ruangan bebas debu
- Setelah kondisi hampir anhidrat tercapai, ganti dengan gliserin 100%
- Lanjutkan ke langkah pemrosesan berikutnya secara langsung
- n-butyl alcohol & t-BUTYL ALCOHOL (Kombinasi dehidrasi dan infiltrasi)
- Metode pertama
- Jaringan langsung dipindah ke paraffin lembut → medium → keras sebelum diembedding ke paraffin. Jaringan dibiarkan lama pada setiap paraffin agar alcohol keluar dari paraffin.
- Metode kedua
- Jaringan dipindahkan ke n-Butyl Alcohol : Parafin keras (1:1) di dalam oven. Campuran dibiarkan beberapa hari hingga alcohol menguap dari paraffin.
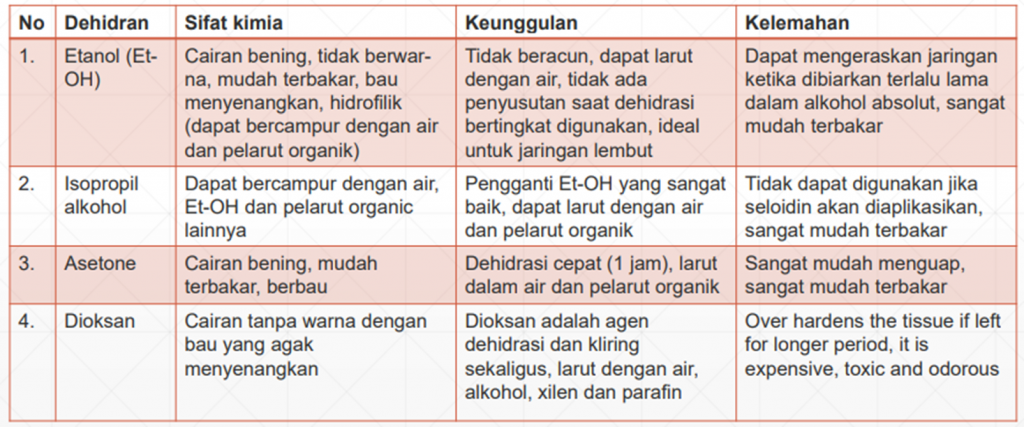
Kelebihan dan Kekurangan Beberapa Dehidrant